支气管哮喘作为高发慢性气道炎症性疾病,重度患者因病情控制不佳、急性发作频繁等问题,承受沉重疾病与医疗负担。在中国,重度哮喘患者以2型炎症为主要表型,现有治疗手段存在覆盖局限、部分患者获益不足等问题。本文聚焦中国重度未控制2型炎症哮喘的诊疗现状与困境,梳理治疗策略演进方向,阐述靶向胸腺基质淋巴细胞生成素(TSLP)的上游阻断方案及其临床价值,为突破治疗瓶颈、优化患者预后提供思路。
现状与挑战:中国重度未控制2型炎症哮喘的高负担与诊疗困境
哮喘的病理本质是慢性气道炎症[1]。随着机制研究的深入,以辅助性T细胞2(Th2)和2型固有淋巴细胞(ILC2)及其分泌的核心细胞因子(如IL-4、IL-5、IL-13)为主导的2型炎症,已被证实是大多数中重度哮喘,特别是重度哮喘的核心病理机制[1]。《支气管哮喘防治指南(2024年版)》[1]指出,满足下列任一指标可作为2型炎症的判断依据:(1)外周血嗜酸性粒细胞(EOS)计数≥150/μL;(2)诱导痰EOS比例≥2.5%;(3)FeNO≥20ppb;(4)过敏原驱动。
在中国重度哮喘患者中,2型炎症表型占据主导地位。研究显示,嗜酸性粒细胞表型占我国重度哮喘患者的比例高达76.8%[2]。与此同时,患者也面临着显著的疾病负担与诊疗挑战。
一项覆盖墨西哥、巴西、哥伦比亚、俄罗斯、土耳其、沙特阿拉伯、阿联酋及中国8个国家、针对12岁及以上哮喘患者的主治医生的横断面调查[3],揭示了我国重度未控制哮喘患者(接受规范高剂量ICS治疗+至少一种控制药物治疗)的疾病负担情况,具体如下:
急性发作频率高:中国亚组(n=102)患者在过去一年内,年均急性发作次数达6.6次(标准差5.8),高于调查总人群的平均水平(4.1次)[3]。
医疗资源占用频繁:中国患者年均急诊就诊次数达6.3次(标准差7.9),年均因急性发作需住院次数达4.9次(标准差4.4)[3]。
炎症水平突出:中国患者外周血平均EOS水平为459.3/μL(标准差310.6),远高于整体研究人群的203.0/μL(标准差265.9)[3]。
共病情况常见:中国患者合并至少一种2型炎症相关共病(过敏性鼻炎、慢性鼻窦炎伴鼻息肉、特应性皮炎)的比例达55.9%[3],增加了疾病诊疗的复杂性。
治疗策略有待优化:调查期间,中国患者中接受生物制剂附加治疗的比例仅为24%[3],提示当时大量符合2型炎症特征的患者可能未能获得前沿的靶向治疗。
综上,我国临床正面临着一个以2型炎症为主要表型、疾病活动度高、共病普遍存在,且迫切需要更有效治疗方案的重度哮喘患者群体,优化该人群的诊疗策略已成为临床亟待解决的重要课题。
机制与局限:从抑制下游特定通路到寻求上游突破的治疗演进
为应对重度哮喘的治疗挑战,靶向特定炎症通路的生物制剂已成为全球哮喘管理指南(GINA)推荐的核心治疗策略。目前,临床应用的生物制剂主要通过阻断2型炎症通路中的特定下游环节发挥作用,具体包括:
抗IgE治疗:通过与血清游离IgE结合,抑制依赖IgE的抗原提呈等,并下调高亲和力IgE受体表达[4,5]。
抗IL-5/IL-5R治疗:通过特异性结合游离IL‑5/IL‑5Rα,抑制IL‑5/IL‑5R信号通路,阻断EOS增殖、分化、招募及存活[6]。
抗IL-4Rα治疗:通过特异性结合IL‑4与IL‑13受体复合物共有的IL‑4Rα亚基,抑制IL‑4和IL‑13的信号转导过程[7]。
上述生物制剂主要干预已分化成熟的免疫细胞或炎症通路中下游相对特定的效应细胞因子,革新了重度哮喘的临床治疗格局,但仍有一些重度2型炎症哮喘得不到控制,因此,临床实践仍在探索可作用于炎症网络上游环节的干预策略。
突破与前景:靶向TSLP,从源头重塑中国重度哮喘的治疗格局
TSLP的发现,为满足上述临床治疗需求提供了新的方向。TSLP主要由气道上皮细胞在受到外界刺激(过敏原、病原体、环境污染物等)后释放,是启动和维持2型炎症反应的核心上游预警素[8],其关键作用主要体现在以下两方面:
启动枢纽:激活树突状细胞,驱动初始T细胞向Th2细胞分化[9];
炎症放大器:促进IL-4、IL-5、IL-13等下游效应细胞因子的产生与释放,促进EOS增多并募集到炎症部位;同时激活肥大细胞,直接诱导其释放细胞因子,共同放大2型炎症信号[9]。
因此,靶向TSLP的治疗策略,意味着在炎症反应的起始环节进行干预,有望从源头调控2型炎症,从而覆盖更广泛的患者群体。
围绕全球首个靶向TSLP的生物制剂特泽利尤单抗开展的DIRECTION临床试验(NCT03927157)带来了新的解答,它是一项多中心、随机、双盲、安慰剂对照的Ⅲ期临床试验,纳入18~80岁重度未控制哮喘患者,按1:1比例随机分配至特泽利尤单抗治疗组或安慰剂组[10]。该研究的事后分析专门评估了270例中国重度未控制2型炎症哮喘患者治疗期间各项终点指标的变化,其中重度未控制2型炎症哮喘的定义为:基线外周血EOS≥150/μL和/或FeNO≥25ppb[10]。
为期52周的随访数据显示:
急性发作明显减少:特泽利尤单抗组136例患者共发生34次哮喘急性发作,安慰剂组134例患者共发生159次急性发作;特泽利尤单抗组年化哮喘急性发作率(AAER)为0.27,显著低于安慰剂组的1.47(RR0.18,95% CI:0.11,0.31,P)[10]。
肺功能持续改善:试验组FEV1相较于基线有明显提升;且其提升幅度全程大于安慰剂组,差异均具有统计学意义(P;图1)[10]。
健康相关生活质量提高:哮喘控制问卷(ACQ-6)评分自第8周起、哮喘生活质量问卷[AQLQ(S)+12]总分自第24周起,改善均显著优于安慰剂组,并持续至研究结束(均P5;图1)[10]。
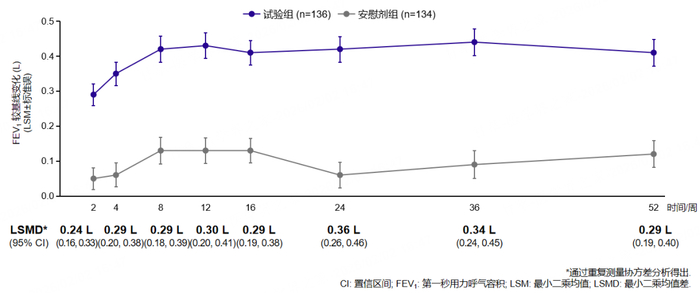
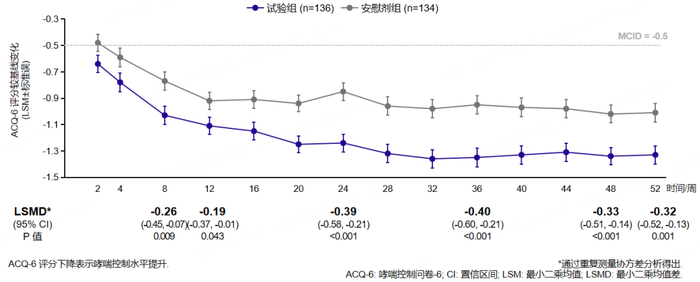
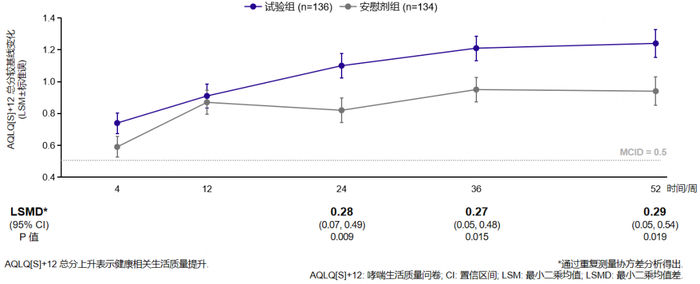
图1:随访期间两组患者肺功能(上)、ACQ-6评分(中)、AQLQ(S)+12(下)总分
值得注意的是,在基线同时伴有血EOS≥150/μL且FeNO≥25 ppb的患者亚组(n=155)中,上述获益更为明确[10]。提示对于中国重度未控制2型炎症哮喘患者(包括接受口服糖皮质激素维持治疗的患者),无论其炎症表型为血EOS和FeNO均升高或是单项升高,特泽利尤单抗均展现出快速且持续的疗效,包括降低急性发作风险、改善肺功能及症状,并提高健康相关生活质量。
结语
中国重度2型炎症哮喘患者疾病负担沉重,以特泽利尤单抗为代表的TSLP抑制剂为中国这一特定人群提供了新的治疗选择。展望未来,临床实践应进一步加强精细表型评估,基于精准分型合理应用可覆盖更广泛炎症谱系的创新药物,将有望改善中国重度哮喘患者的长期预后,实现更高水平的疾病控制目标。
专家简介

王玮 教授
教授、主任医师,博士生/博士后导师
中国医科大学附属一院呼吸与危重症医学科 主任
中华医学会呼吸分会 副主任委员
中国医师协会呼吸医师分会 副会长
中国老年医学学会睡眠分会 副会长
辽宁省医学会呼吸分会 主任委员
辽宁省医师协会内科医师分会 副会长
辽宁省生命科学学会 副会长
辽宁省特聘教授
兴辽英才计划百千万人才领军人才
辽宁省优秀科技工作者
辽宁省本科教学名师
辽宁省三八红旗手
辽宁省最美医务工作者
全国五一劳动奖章获得者
全国先进工作者
参考文献:
[1]中华医学会呼吸病学分会. 支气管哮喘防治指南(2024年版)[J]. 中华结核和呼吸杂志, 2025, 48(3): 208-248.
[2]Zhang Q, Fu X, Wang C, et al. Severe eosinophilic asthma in Chinese C‑BIOPRED asthma cohort. Clin Transl Med, 2022, 12(2): e710.
[3]Kosoy I, Lew E, Ledanois O, et al. Characterization of uncontrolled, severe asthma patients with type 2 inflammation (T2): results from a physician survey across countries from Latin American, Eurasian Middle East regions and China. J Asthma. 2022;59(5):1021-1029.
[4]Brusselle GG, Koppelman GH. Biologic Therapies for Severe Asthma. N Engl J Med, 2022, 386(2): 157‑171.
[5]Pelaia G, Gallelli L, Renda T, et al. Update on optimal use of omalizumab in management of asthma. J Asthma Allergy, 2011, 4: 49‑59.
[6]Agache I, Beltran J, Akdis C, et al. Efficacy and safety of treatment with biologicals (benralizumab, dupilumab, mepolizumab, omalizumab and reslizumab) for severe eosinophilic asthma. A systematic review for the EAACI Guidelines‑recommendations on the use of biologicals in severe asthma[J]. Allergy, 2020, 75(5): 1023‑1042.
[7]Agache I, Song Y, Rocha C, et al. Efficacy and safety of treatment with dupilumab for severe asthma: A systematic review of the EAACI guidelines‑Recommendations on the use of biologicals in severe asthma[J]. Allergy, 2020, 75(5): 1058‑1068.
[8]Gauvreau GM, Sehmi R, Ambrose CS, et al. Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Expert Opin Ther Targets. 2020;24(8):777-792.
[9]黄格格, 甘辉, 朱政. 上皮源预警素在过敏性疾病中的作用机制及研究进展[J]. 中华预防医学杂志, 2025, 59(9): 1381-1389.
[10]金美玲, 杨新艳, 赵立, 等. 特泽利尤单抗在中国T2型炎症重度未控制哮喘患者中的疗效:DIRECTION研究事后分析[R]. 中华医学会变态反应学年会(CSA), 2025.



